Die Arbeitsgruppe »Biologische Materialanalytik« entwickelt präklinische, zellbasierte Testmodelle für die biologische Beurteilung medizinischer Produkte.
Die Entwicklung bio- und immunkompatibler medizinischer Produkte, wie Medizinprodukte und Arzneimittel, erfordert die Betrachtung der Wechselwirkung zwischen Materialien bzw. Wirkstoffen und der Biologie (Biomoleküle, Zellen und Gewebe), um diese sicher am und im Menschen einsetzen zu können.
Die Arbeitsgruppe »Biologische Materialanalytik« verfolgt deshalb einen interdisziplinären Ansatz. An der Schnittstelle von Medizinprodukt- bzw. Arzneimittelentwicklung und Immunbiologie werden Materialien, Substanzen und Wirkstoffe für industrielle Partner bewertet, sowie in Kooperation optimiert oder neu entwickelt. Dafür werden auch standardisierte, diagnostische Screening-Testverfahren entwickelt.
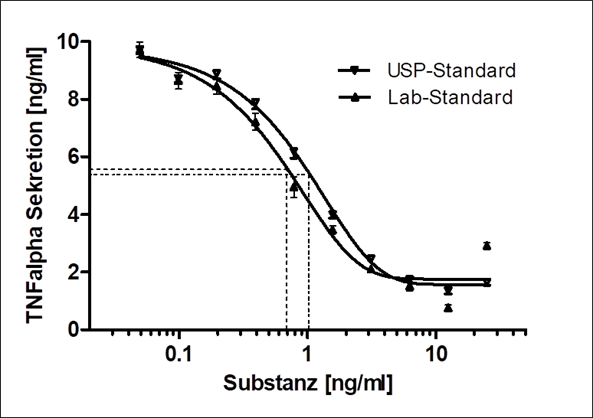
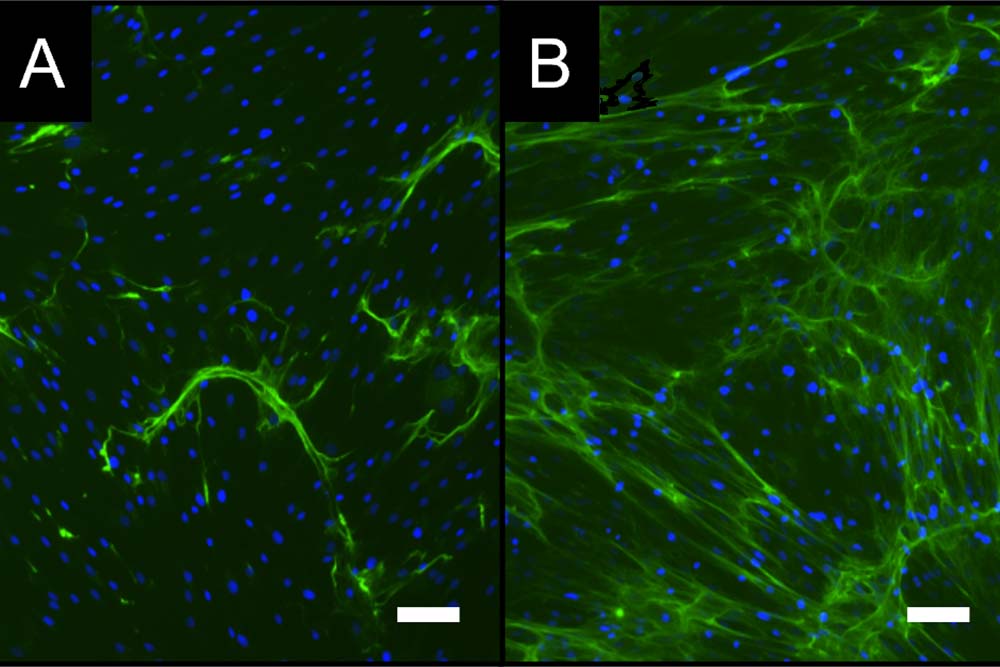
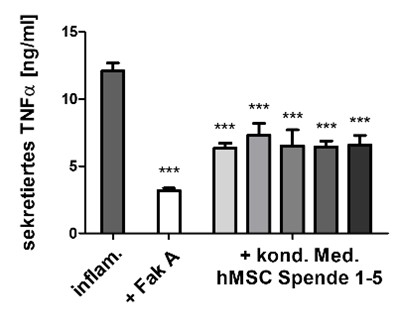
Im Mittelpunkt stehen zellbasierte Testszenarien, Testsysteme und Analyseverfahren für den In-vitro-Einsatz. Die entwickelten Prozesse bilden das Grundgerüst für die zu untersuchenden Fragestellungen. In der Umsetzung liegt der Fokus vor allem auf physiologischen Abläufen, d. h. Prozessen im Patienten. Mit solchen In-vitro-Prüfungen in der präklinischen Phase können die für den jeweiligen Anwendungszweck geeignetsten Materialien/Wirkstoffe zügig und zuverlässig identifiziert, bewertet und somit die Entwicklung neuartiger medizinischer Produkte beschleunigt werden. Den Testszenarien werden passende Annahmekritierien der Methodenentwicklung und -validierung zugrunde gelegt.
Die Fraunhofer IKTS-Arbeitsgruppe hat ihren Arbeitssitz am Fraunhofer-Institut für Zelltherapie und Immunologie IZI in Leipzig. Es bestehen enge Kooperationen zu Arbeitsgruppen am IZI mit dem Ziel Medizinprodukte und Zelltherapeutika für industrielle Anwendungen voranzubringen und entwicklungsbegleitend zu testen.